El carbón activado (AC) se refiere a los materiales altamente carbonosos que tienen alta porosidad y capacidad de sorción producidos a partir de la madera, cáscaras de coco, carbón y conos, etc. El AC es uno de los adsorbentes de uso frecuente utilizados en diversas industrias para la eliminación de numerosos contaminantes de los cuerpos de agua y aire. Dado que el AC se sintetiza a partir de productos agrícolas y de desecho, ha demostrado ser una gran alternativa a las fuentes no renovables y costosas utilizadas tradicionalmente. Para la preparación del AC, se utilizan dos procesos básicos, carbonización y activación. En el primer proceso, los precursores se someten a altas temperaturas, entre 400 y 850 °C, para expulsar todos los componentes volátiles. La temperatura elevada elimina todos los componentes no carbonosos del precursor, como hidrógeno, oxígeno y nitrógeno en forma de gases y alquitranes. Este proceso produce carbón con alto contenido de carbono pero baja área superficial y porosidad. Sin embargo, el segundo paso implica la activación del carbón previamente sintetizado. La mejora del tamaño de los poros durante el proceso de activación se puede clasificar en tres: apertura de poros previamente inaccesibles, desarrollo de nuevos poros mediante activación selectiva y ampliación de poros existentes.
Generalmente, se utilizan dos enfoques, físico y químico, para la activación con el fin de obtener el área superficial y la porosidad deseadas. La activación física implica la activación del carbón carbonizado mediante gases oxidantes como aire, dióxido de carbono y vapor a altas temperaturas (entre 650 y 900 °C). El dióxido de carbono suele ser el preferido debido a su pureza, fácil manejo y un proceso de activación controlable en torno a los 800 °C. Se puede obtener una alta uniformidad de poros con la activación con dióxido de carbono en comparación con el vapor. Sin embargo, para la activación física, se prefiere mucho más el vapor en comparación con el dióxido de carbono, ya que se puede producir carbón activo con un área superficial relativamente alta. Debido al menor tamaño molecular del agua, su difusión dentro de la estructura del carbón se produce de manera eficiente. Se ha descubierto que la activación con vapor es de dos a tres veces mayor que la del dióxido de carbono con el mismo grado de conversión.
Sin embargo, el método químico implica la mezcla del precursor con agentes activadores (NaOH, KOH y FeCl₃, etc.). Estos agentes activadores actúan como oxidantes y deshidratantes. En este método, la carbonización y la activación se llevan a cabo simultáneamente a una temperatura comparativamente más baja (300-500 °C) que en el método físico. Como resultado, se produce la descomposición pirolítica y, posteriormente, la expansión de una estructura porosa mejorada y un alto rendimiento de carbono. Las principales ventajas del método químico sobre el físico son el requisito de baja temperatura, las estructuras de alta microporosidad, la gran área superficial y el tiempo de finalización de la reacción minimizado.
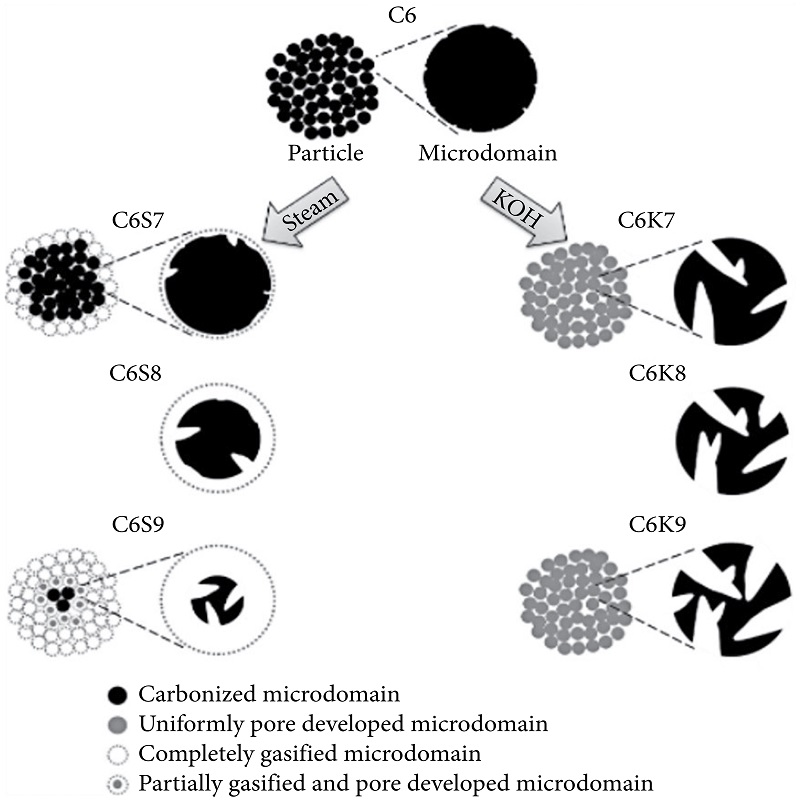
La superioridad del método de activación química se puede explicar con base en un modelo propuesto por Kim y sus colaboradores [1] según el cual se encuentran varios microdominios esféricos responsables de la formación de microporos en el CA. Por otro lado, los mesoporos se desarrollan en las regiones intermicrodominio. Experimentalmente, formaron carbón activado a partir de resina a base de fenol mediante activación química (usando KOH) y física (usando vapor) (Figura 1). Los resultados mostraron que el CA sintetizado por activación con KOH poseía una alta área superficial de 2878 m2/g en comparación con 2213 m2/g por activación con vapor. Además, se encontró que otros factores como el tamaño de poro, el área superficial, el volumen de microporos y el ancho promedio de poro eran mejores en condiciones activadas con KOH en comparación con las activadas con vapor.
Diferencias entre el CA preparado a partir de la activación con vapor (C6S9) y la activación con KOH (C6K9), respectivamente, explicadas en términos del modelo de microestructura.
Según el tamaño de partícula y el método de preparación, se puede clasificar en tres tipos: CA en polvo, CA granular y CA en perlas. El CA en polvo se forma a partir de gránulos finos de 1 mm de tamaño con un diámetro promedio de 0,15-0,25 mm. El CA granular tiene un tamaño comparativamente mayor y una superficie externa menor. El CA granular se utiliza para diversas aplicaciones en fase líquida y gaseosa, dependiendo de su relación dimensional. Tercera clase: el CA en perlas se sintetiza generalmente a partir de brea de petróleo con un diámetro de 0,35-0,8 mm. Es conocido por su alta resistencia mecánica y bajo contenido de polvo. Se utiliza ampliamente en aplicaciones de lecho fluidizado, como la filtración de agua, debido a su estructura esférica.
Hora de publicación: 18 de junio de 2022

